Betrachtung aus pulmonologischer, kardiologischer und neurologischer Sicht
VNR: 2760602023119450006
Dr. med. Peter Kardos, Prof. Dr. med. Axel Schmermund, Prof. Dr. med. Alexandra Henneberg
Einleitung
Das Chronische Fatigue-Syndrom wurde schon lange vor dem Auftreten der Corona-Pandemie beschrieben: Fatigue – chronische Müdigkeit und abnorme Erschöpfbarkeit, die sich durch Schlaf nicht bessern lässt, vielmehr ihrerseits mit Schlafstörungen einhergeht – kann bei chronischen oder nach akuten Infektionen, bei rheumatologischen, endokrinologisch/gynäkologischen, hämatologisch/onkologischen, gastroenterologischen Erkrankungen und in der Neuropsychiatrie als Begleitsymptom einer Multiplen Sklerose, einer Depression, einer Myasthenia gravis, eines Parkinson- oder Alzheimer-Syndroms, einer cervicalen Spinalkanalstenose oder Z. n. Schleudertrauma der HWS oder bei ADHS auftreten (Übersicht in [1]).
Diese Diagnose ist volkswirtschaftlich so bedrückend, dass sich sogar der Deutsche Bundestag bei einer Prävalenz von 250.000 bis 300.000 Personen, darunter 40.000 Kinder und Jugendliche, damit befasst hat [2].
Aus gegebenem Anlass wollen wir uns aber aus der Sichtweise unserer jeweiligen Fachrichtung mit dem Fatigue-Syndrom bei Corona-Patienten im Rahmen eines Long-/Post-Covid-Syndroms beschäftigen, da erwartet wird, dass bis zu 15 % der Infizierten diesen chronischen Verlauf nehmen [3].
Prof. Dr. med. Alexandra Henneberg, Ärztin für Neurologie und Psychiatrie, Praxis Scheffelstr. 31, 60318 Frankfurt
Ein Abkürzungsverzeichnis findet sich am Ende des Beitrags.
Post Covid: Pulmologische Aspekte
Dr. med. Peter Kardos
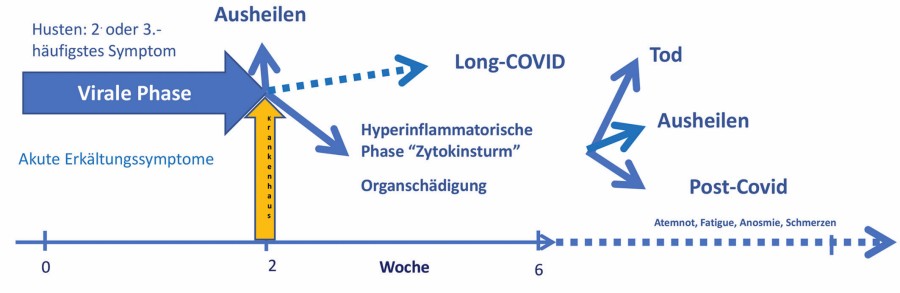
Nach einer meistens durch Aerosol (kleine Teilchen mit einer Größe von < 1 µM) übertragenen aerogenen Infektion kommt es nach einer Inkubationszeit zum Symptombeginn mit einer entzündlichen viralen Phase von ein bis zwei Wochen Dauer, die folgenlos ausheilen kann. Bei einem Teil der Patienten mit schwerem Verlauf tritt ein Zytokinsturm auf, der zu schweren Organschäden mit potenziell letalem Ausgang führen kann (Abb. 1). Bei allen Verlaufsvarianten, auch bei asymptomatischen und leichten [4], kann jedoch ein Post-Covid-Syndrom (PCS) auftreten [5].
PCS ist durch eine Reihe verschiedener Symptome geprägt [6], darunter an prominenter Stelle Atemnot und Fatigue, neben Anosmie und Schmerzen. Weibliches Geschlecht, vorbestehende Fibromyalgie, Migräne, Reizdarm, COPD und Asthma sind häufiger mit Long Covid und Post Covid assoziiert [7].
Da ME/CFS (Myalgische Encephalomyelitis/Chronisches Fatigue-Syndrom) eine Ausschlussdiagnose ist und nach Viruserkrankungen, darunter Covid-19, auftreten kann, regelhaft mit Dyspnoe, Belastungsintoleranz, Schlafstörungen einhergeht [8], ist es aus pneumologischer Sicht wichtig, zwischen Atemnot in Rahmen einer ME/CFS und den pneumologischen Erkrankungen, die bei PCS auftreten können, zu unterscheiden. Im Gegensatz zu der pulmologisch begründeten Belastungsdyspnoe, die charakteristischerweise bei chronisch obstruktiver Lungenerkrankung (COPD), interstitiellen Lungenerkrankungen (ILD), pulmonaler Hypertonie (PH) während der Belastung auftritt, oder zum Belastungsasthma, das in der Regel gegen Ende der Belastung oder Minuten danach in Erscheinung tritt; die für ME/CFS typische Atemnot – Post-Exertional Malaise (PEM) – tritt Stunden oder einen Tag nach der Belastung auf.
Obwohl mehr als 50 verschiedene Post-Covid-Erkrankungen mit verschiedenen Organmanifestationen beschrieben worden sind [9], der typische Post-Covid-Patient hat am häufigsten Fatigue und neurokognitive Defizite und sucht ärztliche Hilfe mit 3–4 Monaten zurückliegendem akutem SARS-CoV-2-Infekt; Dyspnoe und Husten sind dabei der zweithäufigste Symptomkomplex [10].
Zur pneumologischen Abklärung empfiehlt die S1-Leitlinie [5]:
- Klinische Untersuchung, insbesondere die Frage nach kardialer Ursache (falls noch nicht abgeklärt worden).
- Blutdruck, Orthostase-Test.
- Labor: Differenzialblutbild (Anämie?), Transaminasen, Harnstoff, Kreatinin, Elektrolyte, Ferritin, CRP, BSG, D-Dimere, NT-pro-BNP, TSH.
- Lungenfunktionsprüfungen (Spirometrie, Bodyplethysmographie, Diffusion)
- Belastungsuntersuchung: Sechs-Minuten-Gehtest, Spiroergometrie.
- Bildgebung: Die Röntgenaufnahme der Thorakalorgane ist nicht sensitiv für eine SARS-CoV-2-Lungenbeteiligung. Die Spiralcomputertomographie ist aussagekräftig, allerdings um den Preis einer höheren Strahlenbelastung. Typische Veränderungen im CT (periphere multifokale Milchglastrübungen, Plattenatelektasen und septale Fibrosen, seltener erweiterte Bronchien) haben bei der Erstuntersuchung keine therapeutische Konsequenz, da sie nach sechs Monaten in der Regel spontan abklingen [11]. Viele Post-Covid-Patientinnen sind im gebärfähigem Alter. Wir empfehlen die CT-Diagnostik erst nach mehreren Monaten Beschwerdedauer zu veranlassen, da keine unmittelbare therapeutische Konsequenzen bestehen.
- Lungenperfusionsszintigraphie zum Nachweis von peripheren Lungenembolien
Am häufigsten werden bei anhaltender Belastungsdyspnoe keine pathologischen Lungenfunktionsbefunde erhoben. Dann handelt es sich um ME/CFS. Der häufigste Lungenfunktionsbefund, den der Autor bei Post-Covid-Patienten erhebt, ist eine leichte restriktive Ventilationsstörung, auch bei Patienten, die keine Lungenbeteiligung gehabt haben. Die publizierte Evidenz in der Literatur für diesen Befund ist allerdings spärlich [12, 13].
Die akute Lungenbeteiligung bei schwerer SARS-CoV2-Erkrankung ist die häufigste Komplikation [14]. Bei Post-Covid-Patienten klingt die pulmonale Symptomatik häufig nach sechs Monaten ab [15].
In einigen Fällen finden sich folgende pneumologische Erkrankungen bei Post-Covid-Patienten:1
- Lungenbeteiligung bei schwer verlaufenden Sauerstoff- oder beatmungspflichtigen Covid-Patienten interstitielle Lungenveränderungen, die aber auch bei nicht beatmeten Patienten vorkommen können [16]. Interstitielle Lungenerkrankungen sind die häufigsten Folgen von schweren SARS CoV2 Verläufen mit systemischer entzündlicher Antwort und gehen im Akutstadium mit Husten und Hypoxie einher; interessanterweise steht die Dyspnoe nicht im Vordergrund, „happy hypoxia“ genannt [17, 18]. Das radiologische Korrelat sind subpleural und multisegmental lokalisierte Milchglastrübungen, die im Computertomogramm auch bei ambulanten Patienten gesehen werden und Monate persistieren können [19], aber selbst in mittelschweren hospitalisierten Fällen bleiben nach einem Jahr nur selten CT-Veränderungen zurück. Schwerere Formen der interstitiellen Beteiligung bei Post Covid beinhalten verbleibende interstitielle Veränderungen nach Beatmung, ARDS; Lungenfibrose [20, 21, 22].
- In vielen Fällen trifft man radiologisch auf eine organisierende Pneumonie [23, 24]. Eine Verringerung der Diffusionskapazität bei der Lungenfunktionsprüfung sollte Anlass für eine CT-Diagnostik geben [25].
- Verschlechterung/Exazerbation eines zuvor kontrollierten Asthmas wird bei einigen bekannten Asthmapatienten in den ersten drei Monaten nach Covid-19 gesehen [26].
- COPD-Verschlechterung bei Post Covid ist eher ein seltenes Problem [27].
- Dysfunktionale Atmung unter Belastung kann Belastungsdyspnoe verursachen, obwohl die Lungenfunktionstests normal ausfallen. Sie kann bei Spiroergometrie registriert werden: stetig wechselndes Atemzugsvolumen (unregelmäßige, hastige Atmung), oft Hyperventilation [28].
- Dekonditionierung und Gewichtszunahme sind als Auslöser der Long-Covid-Dyspnoe ebenfalls in Betracht zu ziehen [29].
- Abgelaufene Lungenembolien mit und ohne CTEPH. Häufig kann es sich um Thromboembolien der kleinen, peripheren Gefäße handeln, die in kontrastmittelgestützter Computertomografie nicht erkannt werden. Sie können am besten durch eine Perfusionsszintigrafie diagnostiziert werden [5, 30].
- Störungen der peripheren Oxygenierung, Sauerstoffaufnahme in den peripheren Muskeln führt bei normaler Lungenfunktion zur Intoleranz der Belastung und kann nur spiroergometrisch detektiert werden [31].
- Tagesmüdigkeit ist das Kardinalsymptom eines Schlafapnoesyndroms. Die Patienten kommen (oder sie werden geschickt) entweder wegen Schnarchens oder häufig, weil sie tagsüber zum Beispiel bei der Arbeit am Bildschirm, in Sitzungen, bei monotoner Tätigkeit, im Theater, beim Fernsehen, im reizarmen Milieu ungewollt einschlafen. Seltener, insbesondere bei Frauen gehört die Insomnie (Einschlaf- und/oder Durchschlafstörungen) ebenfalls ins Spektrum der Schlafapnoesymptomatik. Letztere kann in ähnlicher Form auch bei Post Covid ME/CFS auftreten. Deshalb ist bei Insomnie in Rahmen von Post Covid ME/CFS eine Schlafdiagnostik indiziert. Eine Einschlafneigung tagsüber ist eher charakteristisch für das Schlafapnoesyndrom und sie kann mit dem Epworth Score quantifiziert werden. Es wird nach der Wahrscheinlichkeit zum Einschlafen bei acht verschiedenen Tätigkeiten gefragt. Beurteilt wird die Einschlafneigung auf einer Skala von 0–3 pro Frage, einem Gesamtscore von 0–24 entsprechend. Ab Score 10 spricht man von Tagesmüdigkeit, über Score 14 von exzessiver Tagesmüdigkeit. Differenzialdiagnostisch gut abgrenzbar hiervon ist die Tagesmüdigkeit bei ME/CFS. Hier handelt es sich um ein Versagen der Leistungsfähigkeit gleichzeitig mit einer fehlenden Erholungsfähigkeit. Eine Einschlafneigung tagsüber gehört nicht dazu [8]. Eine Schlafapnoe kann durch Post Covid ausgelöst oder verschlechtert werden. [32, 33].
Dr. med. Peter Kardos, Gemeinschaftspraxis und Belegarztabteilung Pneumologie, Allergologie, Schlafmedizin; Klinik Maingau vom Roten Kreuz, Frankfurt am Main
Fußnote:
1 Anmerkung: Am 25.10.2022: fanden sich unter den Suchwörtern Long Covid und Post Covid in PubMed 3.280 Publikationen. Es ist daher nur möglich, die Ausführungen zu den einzelnen Erkrankungen beispielhaft mit Publikationen zu belegen.
Post Covid: Kardiovaskuläre Aspekte
Prof. Dr. med. Axel Schmermund
Eine eingeschränkte kardiorespiratorische Fitness ist für viele Patienten mit Myalgischer Enzephalomyelitis bzw. Chronischem Fatigue-Syndrom (ME/CFS) der Anlass, ärztliche Hilfe zu suchen. Umgekehrt gibt es auch Hinweise auf ein erhöhtes Risiko für kardiovaskuläre Erkrankungen bei Patienten mit ME/CFS [33]. Entsprechend wichtig ist der kardiovaskuläre Symptomkomplex und seine Abklärung und Therapie. Eine kürzlich veröffentlichte Übersichtsarbeit von Natelson et al. fasst diese Aspekte sehr gut zusammen und ist die Grundlage für den kardiovaskulären Abschnitt der aktuellen Arbeit [34].
Den Anlass zur kardiologischen Vorstellung betroffener Patienten bietet häufig ein prominentes Symptom, das auch Bestandteil der Definition von ME/CFS ist [35]: Post-Exertional Malaise, PEM. Es kommt zur Verschlechterung des Befindens nach körperlicher (oder geistiger) Anstrengung häufig mit erheblicher zeitlicher Verschiebung, z. B. nach 24 Stunden [35]. Manchmal werden die Patienten auch aufgrund von Symptomen einer orthostatischen Intoleranz vorstellig, die sich z. B. als kognitive Beeinträchtigungen und Sehstörungen in aufrechter Haltung bemerkbar machen. Erwartungsgemäß sind die Beschwerden und Symptome für sich genommen schwer fassbar und nicht spezifisch. In der Kombination sind sie aber anhand der vorgegebenen Diagnosekriterien wegweisend [35].
Aus kardiovaskulärer Sicht lassen sich bei der gezielten Untersuchung von Patienten mit ME/CFS pathophysiologische Besonderheiten finden, die vor allem fünf Bereiche betreffen (siehe Tabelle 1).
Tabelle 1: Kardiovaskuläre Auffälligkeiten bei ME/CFS |
|
|
|
|
|
1) Rückgang von Herzgröße und Blutvolumen ähnlich wie bei Dekonditionierung und Alterungsprozessen
Übereinstimmend wurde in mehreren Studien ein erniedrigtes Schlagvolumen bei ME/CFS im Vergleich mit Normalpersonen dokumentiert, niedrigere endsystolische und enddiastolische Volumina des linken Ventrikels sowie auch ein Rückgang der Wanddicken [34]. Zudem fand sich ein erniedrigtes Blut- oder Erythrozytenvolumen. Sowohl die Parameter der Herzgröße wie auch das Blutvolumen schienen in linearem Zusammenhang mit dem Schweregrad des ME/CFS zu stehen. Daneben wurde eine fehlende Anpassung der Vorlast bei Anstrengung beschrieben und somit eine Störung der Frank-Starling-Reaktion. Die Befunde weisen insgesamt Ähnlichkeiten mit dem physiologischen Alterungsprozess auf [36]. Es scheint einen Rückgang des Schlag- und Blutvolumens bei ME/CFS zu geben, möglicherweise bedingt durch eine eingeschränkte Frank-Starling-Reaktion bei fehlender venöser Kompression und aggraviert durch Trainingsmangel/Dekonditionierung [34].
2) Niedrige Blutdruckwerte vor allem über Nacht.
Die Studienergebnisse sind nicht einheitlich, weisen aber in der Mehrzahl auf einen nachts akzentuierten übernormalen Abfall sowohl der systolischen wie auch der diastolischen Blutdruckwerte hin [34]. Es liegt nahe, die Fehlregulation des Blutdrucks in Verbindung mit Fatigue zu bringen und dies auch als Ausdruck der autonomen Dysfunktion einzuordnen, die weiter unten noch ausgeführt wird.
3) Autonome Funktionsstörungen in der Herzfrequenzvariabilität (HRV)
Bei Patienten mit ME/CFS scheint es nachts zu einer vermehrten sympathischen Aktivierung zu kommen, die möglicherweise die fehlende Erholung in der Schlafphase erklärt [34]. Eine reduzierte HRV lässt sich zudem bei orthostatischer Belastung im Rahmen einer Kipptischuntersuchung nachweisen, sowie auch bei Wechsel zwischen Sitzen und Stehen. Der Schweregrad der Fatigue-Symptome scheint mit den Auffälligkeiten in der HRV-Analyse korreliert zu sein [34].
4) Orthostatische Intoleranz mit Symptomverschlechterung in aufrechter Haltung sowie Hypokapnie
Sowohl eine autonome Funktionsstörung als auch ein reduziertes Blutvolumen könnten erklären, warum ME/CFS-Patienten häufig über orthostatische Beschwerden mit Symptomverschlechterung in aufrechter Haltung klagen. Darüber hinaus tritt bei einigen Patienten ein posturales Tachykardiesyndrom (POTS) mit Herzfrequenzbeschleunigung im Stehen um > 30/min oder auf > 120/min auf. POTS scheint weit überwiegend bei Jugendlichen und jungen Erwachsenen mit ME/CFS vorzuliegen, weniger dagegen bei Älteren [34]. Möglicherweise definiert das Vorliegen von POTS eine spezifische Pathophysiologie in einer Untergruppe von ME/CFS-Patienten. Bei einer anderen Untergruppe konnte ein posturales orthostatisches Syndrom der Hypokapnie (POSH) dokumentiert werden. Normalerweise führt eine aufrechte Haltung zur Verminderung des venösen Rückflusses (venöses Pooling), was beim Gesunden kompensatorisch zum einen über Barorezeptoren eine sympathische Aktivierung mit Tachykardie und Vasokonstriktion bewirkt und zum anderen über Chemorezeptoren eine Hyperkapnie. Diese Kompensationsmechanismen sind bei POTS und POSH gestört [34]. Wenngleich die Datenlage nicht einheitlich ist, fällt die Analogie zwischen POTS und POSH-Mechanismen mit einer Dekonditionierung bei Trainingsmangel auf. Tatsächlich scheint sich mit vorsichtig dosiertem Training eine Besserung erzielen zu lassen.
5) Symptomverschlechterung nach körperlicher (oder geistiger) Anstrengung: Post-Exertional Malaise, PEM
Die aggravierten Beschwerden nach oftmals nur leichter körperlicher oder sogar geistiger Anstrengung führen Patienten mit ME/CFS nicht selten zum Kardiologen. Teilweise liegen ein bis mehrere Tage zwischen der Belastung und der Symptomverschlechterung. Es liegt nahe, dieses Phänomen der Verschlechterung nach Anstrengung, Post-Exertional Malaise (PEM), mittels serieller kardiopulmonaler Belastungstests (CPET) zu analysieren. Einige Untersuchungen zeigten bei zwei CPET mit einem Intervall von 24 Stunden einen Rückgang der maximalen Sauerstoffaufnahmekapazität und der anaeroben Schwelle, während Gesunde in der Regel bedingt durch Lern- und Gewöhnungseffekte beim Wiederholungstest besser abschneiden. Ob somit dank serieller CPET eine Art biologischer Marker für ME/CFS vorliegt, bleibt zurzeit aber noch offen [34].
Zusammenfassung
Es lassen sich bei ME/CFS-Auffälligkeiten des kardiovaskulären Systems feststellen, die zumindest teilweise Symptomatik und Krankheitsgefühl erklären. Das betrifft vor allem ein vermindertes Herzzeitvolumen in Ruhe als Folge eines reduzierten Schlagvolumens, einen Rückgang des Blutvolumens sowie Veränderungen der Herzfrequenzvariabilität, verbunden mit posturaler Hypotonie. Vermutlich spielt auch eine Dekonditionierung eine Rolle, wie sie typischerweise in der Folge eines Trainingsmangels z. B. nach durchgemachtem Infekt auftritt. Als Folge der Covid-19-Pandemie wird eine deutliche Zunahme an ME/CFS-Fällen erwartet. Post Covid-Patienten mit ME/CSF leiden offenbar besonders unter posturaler Tachykardie und Hypotonie [37]. Die weltweite Prävalenz von ME/CFS wird aktuell auf 0,3–0,8 % eingeschätzt und dürfte in der nächsten Zeit deutlich ansteigen.
Prof. Dr. med. Axel Schmermund, MVZ CCB Frankfurt und Main-Taunus, Cardioangiologisches Centrum Bethanien, Frankfurt am Main
Post Covid: Neuropsychiatrische Aspekte
Prof. Dr. med. Alexandra Henneberg
Drei Monate nach einer Corona-Infektion liegen noch Symptome vor? Hierzu gehören Fatigue, Kopf- und Muskelschmerzen, Dyspnoe und kognitive Störungen, die mindestens schon für zwei Monate vorhanden sind? Dann ist ein Post-Covid-Syndrom (PCS) wahrscheinlich, das in 15 % aller Infizierten erwartet wird.
Für ein chronisches Fatigue-Syndrom gehören zu den unverzichtbaren Hauptkriterien
- Deutliche Einschränkungen der sozialen, beruflichen/schulischen und persönlichen Aktivitäten über mehrere Monate
- PEM, das heißt schon bei geringer Anstrengung kommt es zu Muskelschmerzen, Schwäche, kognitiven Einschränkungen oder Müdigkeit
- Ein- und/oder Durchschlafstörungen.
Und als Nebenkriterium mindestens ein Zusatzsymptom
- Kognitive Einschränkungen (Arbeitsgedächtnis gestört, Reaktionszeit verlängert, Aufmerksamkeit reduziert) oder
- Orthostatische Dysfunktion, Schwindel, Übelkeit, Palpitationen
(Canadische Consensus-Criterien CCC 2003, zit. nach [38])
Da von anderen Fatigue-Patientinnen und -Patienten bekannt ist, dass es für längere Zeit zu Arbeitsunfähigkeit ggf. Erwerbsunfähigkeit kommen kann, wurde von mir im III. Quartal 2022 eine Befragung in meiner Praxis durchgeführt mit Fragen nach komplikationslosem Verlauf (U08.9Z), durchgemachtem PCS (U09.9Z), noch bestehendem Long-Covid-Syndrom (U09.9 !) oder gar einem fulminanten Verlauf mit Polyarthritis und schwerer Dyspnoe/kardiologischen oder pulmonologischen Komplikationen (U10.9G), dies in Bezug auf vorher erfolgte Impfungen.
Von 1.180 befragten Patientinnen und Patienten waren 172 von einer Infektion betroffen, 26 Patientinnen und 33 Patienten mit unkompliziertem Verlauf, 16 Patientinnen und 14 Patienten mit abgeschlossenem PCS, 56 Patientinnen und 21 Patienten mit andauerndem PCS und 5 Patientinnen und ein Patient mit schweren Komplikationen.
Eine Relation zu vorab erfolgten Immunisierungen zeigt Tab. 2.
Tabelle 2: Relation Long-/Post-Covid zu vorab erfolgten Immunisierungen | |||||||
Diagnose | 4 x B | 3 x B | 2 x B | 1 x B | Mix | keine Impf. | ? |
U08.9Z | 3 | 12 | 4 | 2 | 27 | 6 | 5 |
U09.9Z | 2 | 8 | 2 | 1 | 13 | 3 | 1 |
U09.9 ! | 5 | 6 | 8 | 2 | 27 | 10 | 19 |
U10.9 G |
| 1 |
|
| 3 | 1 | 1 |
U08.9Z: Z. n. Coronainfektion; U09.9Z: Z. n. Long-Covid-Syndrom (Fatigue abgeklungen nach vier bis sechs Monaten); U09.9 ! Long-Covid-Syndrom; U 10.9 G: Multisystemisches Entzündungssyndrom in Verbindung mit Covid-19. B = Biontech. Mix-Immunisierungen: Darunter sind Impfungen mit Astra-Zeneca, Biontech, Johnson und Moderna, die kombiniert wurden, zu verstehen. Reine Impfungen anderer Hersteller als Biontech wurden nicht berichtet. ? = Impfstatus nicht bekannt. | |||||||
Die Diagnose ist lediglich durch die Anamnese zu stellen, wenngleich vom IMD-Labor der Charité Berlin ein Anstieg der beta1- und beta2-adrenergen Autoantikörper bei einem Teil der Patienten berichtet wird, bei anderen ein Anstieg der M3-/M4-muskarinergen Anticholinrezeptor-Autoantikörper. Dies sind wissenschaftliche Ansätze, die zur Zeit noch nichts zur Diagnosestellung beitragen können. Auch Autoantikörper gegen Neuronensomata, Endothel und Neuropil im Bulbus olfactorius und Hippocampus und gegen Körnerzellen des Kleinhirns oder Astrozyten wurden bei PCS-Patienten gefunden, bislang gibt es keine Unterklassifikation (Prüß zitiert nach [39]). Komorbiditäten mit Depression, Angststörungen und psychosozialen Belastungssituationen sind häufig, nach schwerwiegendem Verlauf auf der Intensivstation auch PTBS und Critical Illness Polyneuropathie [38].
Überforderung vermeiden
Betroffene können nach den Neurologischen S2K-Leitlinien der Deutschen Gesellschaft für Neurologie, zuletzt vom 2.8.22 durch [40], bislang nicht kausal, nur symptomatisch behandelt werden, das Wichtigste ist ein jeweils für den Einzelnen individuell herausgefundener Grad der Belastbarkeit („Pacing“), da es bei Überforderung zu einer schnellen Verschlechterung des Krankheitsbildes kommen kann. Dies darf nicht mit einer psychogenen Ursache des Fatigue-Syndroms verwechselt werden, die inzwischen nicht mehr vertreten werden kann [41]. Dennoch gibt es vielversprechende Ansätze der Grundlagenforschung, die von einem Mastzellenaktivierungssyndrom mit Anstieg der Interleukine Il-1 und Il-6 ausgehen und natürliche Stärkung der Mikrogliazellen zur Anregung von Reparaturmechanismen beispielsweise durch Flavonoide wie beispielsweise Luteolin befürworten [42]. Weitere Forschung erscheint dringend angebracht.
Prof. Dr. med. Alexandra Henneberg, Dr. med. Peter Kardos, Prof. Dr. med. Axel Schmermund, Kontakt zu den Autoren: henneberg-neuropsych@t-online.de
Abkürzungsverzeichnis | |
ADHS | Aufmerksamkeitsdefizit-Hyperaktivitätsstörung |
ARDS | akutes Atemnotsyndrom |
BSG | Blutsenkungsgeschwindigkeit |
CFS | Chronisches Fatigue-Syndrom |
COPD | chronisch obstruktive Lungenerkrankung |
CPET | serielle kardiopulmonale Belastungstests |
CRP | C-reaktives Protein |
CTEPH | chronisch thromboembolische pulmonale Hypertonie |
D-Dimere | Spaltprodukte des Fibrins, hohe Werte geben Hinweise auf Thrombosen oder eine Lungenembolie |
HRV | Herzfrequenzvariabilität |
HWS | Halswirbelsäule |
ILD | Interstitielle Lungenerkrankungen |
IMD-Labor | Institut für medizinische Diagnostik |
ME | Myalgische Enzephalomyelitis |
NT-pro BNP | N-terminales pro B-Typ natriuretisches Peptid/Laborparameter zur Diagnostik, Prognose- und Risikoeinschätzung der Herzinsuffizienz |
PCS | Post Covid-Syndrom |
PEM | Postexertionelle Malaise oder Post-Exertional Malaise |
PH | pulmonale Hypertonie |
POTS | posturales Tachykardiesyndrom |
POSH | posturales orthostatisches Syndrom der Hypokapnie |
TSH | Thyreoidea-stimulierendes Hormon, es reguliert die Bildung der Schilddrüsenhormone. |
Multiple Choice-Fragen
Die Multiple Choice-Fragen zu dem Artikel „Fatigue-Syndrom bei Covid-19-Patienten ... Betrachtung aus pulmonologischer, kardiologischer und neurologischer Sicht“ von Dr. med. Peter Kardos, Prof. Dr. med. Axel Schmermund und Prof. Dr. med. Alexandra Henneberg finden Sie im PDF am Ende dieser Seite unter „Artikel herunterladen“ und im Mitglieder-Portal (https://portal.laekh.de). Die Teilnahme zur Erlangung von Fortbildungspunkten ist ausschließlich online über das Mitglieder-Portal vom 25. Februar 2023 bis 24. August 2023 möglich. Die Fortbildung ist mit zwei Punkten zertifiziert. Mit Absenden des Fragebogens bestätigen Sie, dass Sie dieses CME-Modul nicht bereits an anderer Stelle absolviert haben. Dieser Artikel hat ein Peer-Review-Verfahren durchlaufen. Nach Angaben der Autoren sind die Inhalte des Artikels produkt- und/oder dienstleistungsneutral, es bestehen keine Interessenkonflikte.
Die Literaturhinweise finden Sie am Ende dieser Seite unter „Artikel herunterladen“ in der PDF-Version dieses Artikels.