Dr. med. Gunther Rexroth, Martin Rapp, Vera Reinhard
Zusammenfassung
Die bevölkerungsbezogene Krebsregistrierung in Deutschland hat sich in den vergangenen Jahren über die reine Bereitstellung epidemiologischer Tumordaten hinaus entwickelt. Moderne Krebsregister dienen der epidemiologischen Ursachenforschung von Malignomen, dem Monitoring und der Evaluation von Früherkennungsprogrammen und auch der vergleichenden Beurteilung von Tumortherapien. Inwieweit Krebsregister diesen Aufgaben gerecht werden, hängt von der Qualität der eingehenden Daten und den intern praktizierten Mechanismen der Qualitätskontrolle ab.
Der vorliegende CME-Artikel soll einen Überblick über die Arbeit des Hessischen Krebsregisters geben und zugleich eine freundliche Aufforderung an alle praktizierenden Ärzte sein, ihrer gesetzlichen Pflicht nachzukommen, die Daten ihrer Tumorpatienten an das Register zu melden. Leser sollen nach der Lektüre Grundkenntnisse über Verfahren und Nutzen der Krebsregistrierung erlangt haben und sich motiviert fühlen, selbst als Melder aktiv zu werden.
Einleitung
Die Bedeutung der modernen Krebsregistrierung ergibt sich aus ihren Möglichkeiten, die Erkennung und Behandlung von Krebserkrankungen in der Bevölkerung positiv zu beeinflussen. Um dieser Aufgabe gerecht zu werden, ist sie einerseits auf die Qualität der eingehenden Daten und andererseits auf beständige Qualitätssicherungsmaßnahmen angewiesen.
Gesetzliche Grundlagen
Das am 01.01.1995 in Kraft getretene Krebsregistergesetz (KRG) verpflichtete alle Bundesländer zum Aufbau epidemiologischer Krebsregister, um eine Datengrundlage für die Krebs-Epidemiologie zu schaffen und damit die Krebsbekämpfung zu verbessern. Den Bundesländern wurde bis zum 01.01.1999 Zeit gegeben, durch Landesgesetze flächendeckend bevölkerungsbezogene Krebsregister einzurichten (Bundesgesetzbl., 1994).
2008 wurde vom Bundesgesundheitsministerium, der Deutschen Krebsgesellschaft, der Deutschen Krebshilfe und der Arbeitsgemeinschaft Deutscher Tumorzentren e. V. (ADT) zur Verbesserung der onkologischen Versorgung in Deutschland der Nationale Krebsplan aufgestellt. Durch das am 03.04.2013 erlassene Gesetz zur Weiterentwicklung der Krebsfrüherkennung und zur Qualitätssicherung durch klinische Krebsregister (Krebsfrüherkennungs- und -registergesetz, KFRG) wurden die Bundesländer zur Einrichtung klinischer Krebsregister verpflichtet (Bundesgesetzbl., 2013, auch § 65c SGB V).
In Hessen wurden die bundesrechtlichen Vorgaben mit dem Hessischen Krebsregistergesetz (HKRG) am 17.12.2001 umgesetzt, das zwischenzeitlich zweimal novelliert wurde und jetzt in der Fassung vom 19.12.2019 gültig ist.
Organisation
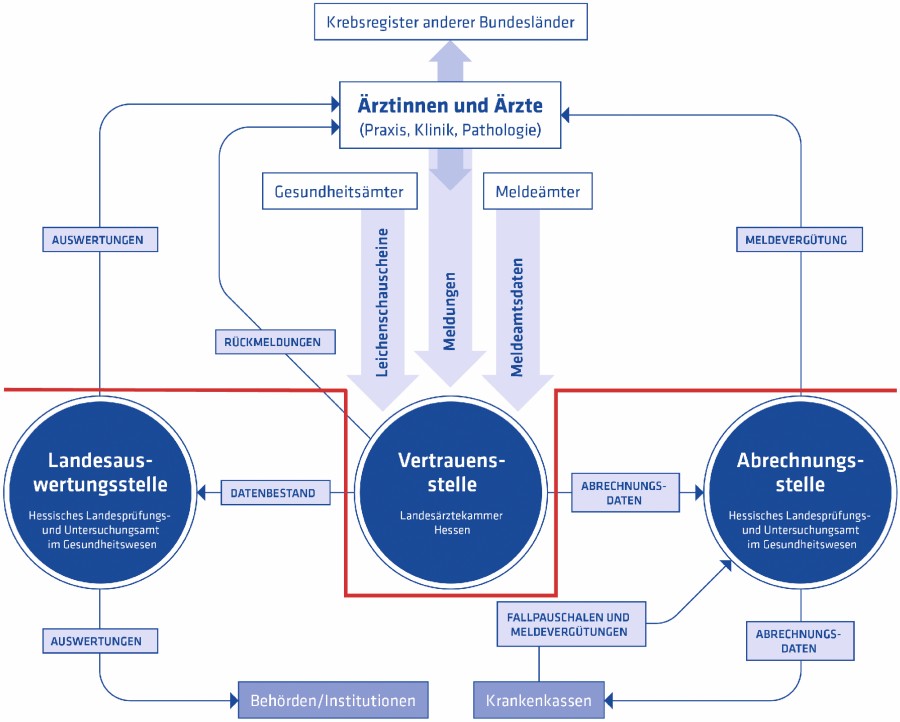
Das Hessische Krebsregister besteht aus der Vertrauensstelle, der Landesauswertungsstelle und der Abrechnungsstelle. Träger des Hessischen Krebsregisters ist das Land. Die Vertrauensstelle ist bei der Landesärztekammer Hessen angesiedelt. Sie nimmt die Rohdaten der onkologisch tätigen Ärzte und Klinikabteilungen, der Gesundheits- und Meldeämter und von Krebsregistern anderer Bundesländer entgegen, führt sie zusammen, prüft sie auf Vollständigkeit und Plausibilität und gibt sie schließlich in pseudonymisierter Form an die Landesauswertungsstelle weiter. Die Vertrauensstelle ist innerhalb der Landesärztekammer Hessen fachlich unabhängig. Die Landesauswertungsstelle und die Abrechnungsstelle sind beim Hessischen Landesprüfungs- und Untersuchungsamt im Gesundheitswesen (HLPUG) angesiedelt und räumlich, organisatorisch und personell von der Vertrauensstelle getrennt (Abb. 1). Die Landesauswertungsstelle wertet die erhaltenen Daten aus, erstellt epidemiologische und klinische Krebsberichte und führt (regionale) Qualitätskonferenzen durch. Die Abrechnungsstelle rechnet Fallpauschalen und Meldevergütungen mit den Krankenkassen ab und zahlt Vergütungen an die meldenden Einrichtungen aus.
Die Aufgaben der Vertrauensstelle und der Landesauswertungsstelle sowie die Abrechnungsdetails sind durch die Verordnung zum HKRG vom 05.10.2015 geregelt.
Abb. 1: Organisation des Hessischen Krebsregisters: Durch die Trennung (rote Trennlinie) in die Vertrauensstelle einerseits und die Auswertungsstelle andererseits werden die Vorgaben des Datenschutzgesetzes gewahrt.
Aufgaben
Das Hessische Krebsregister erfüllt die Aufgaben eines epidemiologischen und eines klinischen Registers. Die epidemiologische Registrierung erfolgt, um das Krebsgeschehen in Hessen im zeitlichen und regionalen Verlauf darzustellen. Daraus können regionale Krebsrisiken (z. B. erhöhte Pleuramesotheliomprävalenz in der Umgebung früherer asbestverarbeitender Betriebe) und zeitliche Veränderungen (z. B. geringere Mortalität von Kolonkarzinomen durch Inanspruchnahme der Vorsorgekoloskopie) abgeleitet werden.
Die klinische Registrierung dient durch Erfassung von Behandlungs- und Verlaufsdaten der Verbesserung der onkologischen Versorgung. Die Auswertungen werden einerseits zur Eigenkontrolle an die Leistungserbringer zurückgemeldet und andererseits mit Ergebnissen aus Studien, Leitlinien und anderen (Bundes-)Ländern verglichen.
Meldepflicht und Meldeanlässe
Nach § 4 Abs. 6 HKRG sind alle in Hessen tätigen Ärztinnen und Ärzte sowie Zahnärztinnen und Zahnärzte meldepflichtig.
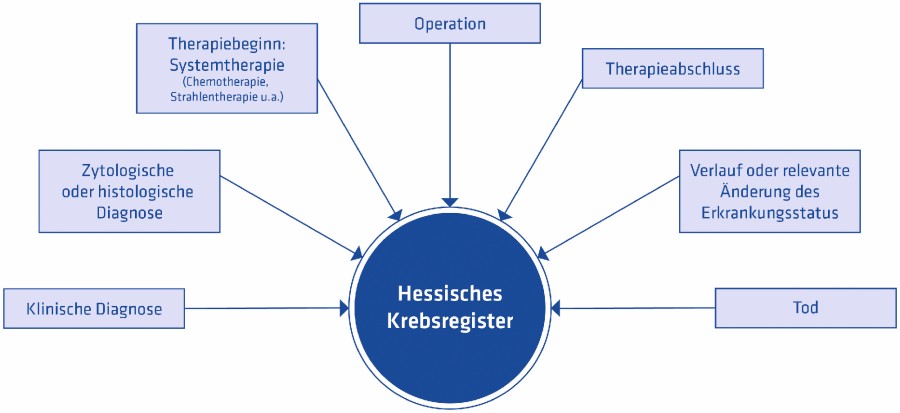
Meldeanlässe sind (Abb. 2):
- die Diagnose einer Tumorerkrankung,
- die histologische, zytologische und autoptische Sicherung der Diagnose,
- der Beginn sowie der Abschluss einer therapeutischen Maßnahme,
- Änderungen im Krankheitsverlauf, insbesondere durch das Auftreten von Rezidiven, Metastasen und Zweittumoren,
- das Ergebnis der Nachsorge,
- der Tod der Patientin oder des Patienten.
In Hessen stehen für die elektronische Datenübermittlung zwei Wege zur Verfügung: die internetbasierte Meldung über ein Meldeportal und (für große Einrichtungen) der Meldeportal-UploadClient (MUC), der die Installation eines JAVA-gestützten Software-Pakets voraussetzt.
Der Melder muss die an Krebs Erkrankten über die Meldung an die Vertrauensstelle unterrichten. Für Pathologen und andere, rein diagnostisch Tätige gilt eine Ausnahmeregelung: Da sie keinen direkten Patientenkontakt haben, dürfen sie die notwendige Unterrichtung des Patienten/der Patientin an den behandelnden Arzt/die behandelnde Ärztin delegieren (§ 5 Abs. 6 des HKRG).
Die Gesundheitsämter sind nach § 6 HKRG verpflichtet, der Vertrauensstelle eine Kopie aller Todesbescheinigungen (vertraulicher Teil) zu übermitteln.
Was muss gemeldet werden?
Es werden im Wesentlichen folgende Daten erfasst:
Identitätsdaten:
- Familiennamen, Vornamen, frühere Namen
- Geschlecht
- Geburtsdatum
Stammdaten:
- Anschrift
- Datum der ersten Tumordiagnose
- Sterbedatum
- Versichertennummer
- Name und IK-Nummer der Krankenkasse
Epidemiologische Daten:
- Geschlecht
- Monat und Jahr der Geburt
- Wohnort mit Postleitzahl
- Straße und Hausnummer
- Tumordiagnose im Klartext und nach dem Schlüssel der Internationalen Klassifikation der Krankheiten (aktuell ICD-10) in der jeweils neuesten vom Deutschen Institut für medizinische Dokumentation (DIMDI) herausgegebenen Fassung. In Hessen sind meldepflichtig:
- alle bösartigen Tumore außer den nicht melanotischen Hauttumoren
- Frühstadien (Carcinoma in situ)
- Gutartige ZNS-Tumore
- Histologie und Lokalisation des Tumors einschließlich der Seite bei paarigen Organen im Klartext und nach dem Schlüssel der Internationalen Klassifikation der onkologischen Krankheiten (ICD-O)
- Monat und Jahr der ersten Tumordiagnose
- Tumorausprägung zum Zeitpunkt der Meldung (Tumornachweis, Primärdiagnostik, Rezidiv, Nachsorge, fraglicher Befund)
- Frühere Tumorleiden
- Stadium der Erkrankung (insbesondere der TNM-Schlüssel zur Darstellung der Größe, des Lymphknotenbefalls und des Metastasierungsgrades der Tumoren)
- Art der Sicherung der Diagnose (klinischer Befund, Histologie, Zytologie, Obduktion u. a.)
- Art der Primärtherapie (kurativ oder palliativ; operative, Strahlen-, Chemo- oder andere Therapie)
- Sterbemonat und Sterbejahr
- Todesursache und Angabe darüber, ob der Tod tumorbedingt war
- Ergebnis der durchgeführten Autopsie
- Datum der Meldung an die Vertrauensstelle
Klinische Daten sind:
- Die o. g. epidemiologischen Daten.
- Alle im bundesweit einheitlichen Datensatz der Arbeitsgemeinschaft Deutscher Tumorzentren (ADT) und der Gesellschaft der epidemiologischen Krebsregister in Deutschland (GEKID) zur Basisdokumentation für Tumorkranke und ihn ergänzender Module aufgeführten Merkmale in der jeweils gültigen Fassung.
- Bei einer Teilnahme an einer Reihenuntersuchung für Krebs das Screeningdatum, das Screeningergebnis sowie gegebenenfalls die Bewertung einer im Zeitraum zwischen zwei Screeninguntersuchungen aufgetretenen Tumorerkrankung (Intervallkarzinom).
In Hessen tätige Ärzte sind dazu verpflichtet, alle von ihnen behandelte Tumorpatienten unabhängig von ihrem Wohnsitz an das Hessische Krebsregister zu melden. Für die epidemiologische Registrierung ist der Hauptwohnsitz entscheidend, für die klinische Registrierung der Behandlungsort. Durch die zunehmende Mobilität der Bevölkerung bedingt, können der Wohnort, der Ort der primären Diagnostik und der Behandlungsort durchaus in verschiedenen Bundesländern liegen. Der Datenaustausch zwischen den Registern der Bundesländer (sog. RÜD = Registerübergreifender Datenaustausch) zum Zwecke der Datenzusammenführung ist daher unerlässlich.
Dokumentationsstandards
Damit die flächendeckenden Krebsregister nach § 65c SGB V ihre Aufgaben erfüllen können, ist die standardisierte Dokumentation der gemeldeten Krebserkrankungen und ihrer Verläufe erforderlich.
Die Krankheiten werden nach der „Internationalen Klassifikation der Krankheiten und verwandter Gesundheitsprobleme“ (ICD, aktuell in der 10. Revision und in einer auf das deutsche Gesundheitssystem angepassten Fassung) der Weltgesundheitsorganisation (WHO) und der „Internationalen Klassifikation der Krankheiten für die Onkologie (ICD-O) kodiert. Mit der ICD-O-Kodierung (aktuell in der revidierten Fassung der 3. Auflage) werden sowohl der Sitz des Tumors (Topografie) als auch die Gewebeart (Morphologie) verschlüsselt. Leider stimmen die Schlüsselnummer der ICD-10 und der topografische Schlüssel der ICD-O nicht immer überein. Eine umfangreiche Revision der ICD-10 wird derzeit von der WHO erarbeitet.
Zur Beschreibung der Ausdehnung solider Tumore wird die TNM-Klassifikation (aktuell in der 8. Auflage) benutzt. Für systemische Malignome wie Leukämien oder Lymphome sind spezifische Klassifikationen wie z.B. die Ann-Arbor-Klassifikation anzuwenden.
Der in Deutschland durch das Deutsche Institut für Medizinische Dokumentation und Information (DIMDI) herausgegebene Operationen- und Prozedurenschlüssel (OPS) wird zur einheitlichen Kodierung von Operationen, Prozeduren und allgemeinen medizinischen Maßnahmen benutzt.
„Best of“-Verfahren
Sofern aus unterschiedlichen Quellen Meldungen zu einem Sachverhalt kommen, müssen sie nach vorgegebenen Regeln zu einer bestmöglichen Information zusammengefasst werden. Bestehen nur graduelle Unterschiede zwischen den Meldungen, so wird man die genaueste wählen (z. B. ist die Angabe eines Zökumkarzinoms der eines Kolonkarzinoms vorzuziehen). Bei der Beurteilung des TNM-Stadiums ist das vom Pathologen am Resektat gewonnene Stadium (pTNM) besser als das präoperativ klinisch abgeschätzte Stadium (cTNM). Zudem kann sich mit zunehmender Zahl angewandter diagnostischer Verfahren die Qualität einer Diagnose im zeitlichen Verlauf verbessern (z. B. Fortschritt von einem primär diagnostizierten „cancer of unknown primary“ zu einem definierten Primärtumor). Beim Sterbedatum gilt die Angabe des Melderegisters als die zuverlässigste.
Vollzähligkeit
Zur Ermittlung der „tatsächlichen Zahl“ der von einer Tumorentität Betroffenen können sowohl der Vergleich mit Abrechnungsdaten der Krankenkassen als auch von der International Agency for Research on Cancer (IARC) veröffentlichte Schätzverfahren herangezogen werden (Parkin et al., 2009).
Semiquantitativ kommen zum Abgleich z. B. Inzidenzraten oder der Quotient Mortalität/Inzidenz zur Anwendung. Der Quotient lässt sich bei konstantem Krankheitsverlauf wiederum mit der Differenz (1-Wahrscheinlichkeit für das 5-Jahresüberleben) gut abschätzen.
Auch der Anteil der histologisch bestätigten Fälle lässt Rückschlüsse zu: Wenn dieser Anteil unverhältnismäßig hoch ist, spricht das gegen eine vollzählige Erfassung; stattdessen hat man sich zu sehr auf die Meldungen der Pathologie an das Krebsregister verlassen.
Quantitativ kann die Rate der mit dem Leichenschauschein erstmals erkannten Krebserkrankungen (sog. DCN-Fälle, death certificate notified) oder solcher Fälle, von denen auch nach Ermittlungsversuchen nur der Leichenschauschein vorlag (sog. DCO-Fälle, death certificate only), als Anhalt für die Unvollständigkeit eines Registers dienen.
Bei Krebserkrankungen mit geringer Sterblichkeit ist der DCO-Index allerdings wenig aussagekräftig. Zudem ist der Index durch die recht hohe Fehlerrate der Angaben auf Leichenschauscheinen limitiert (Brenner, 1995).
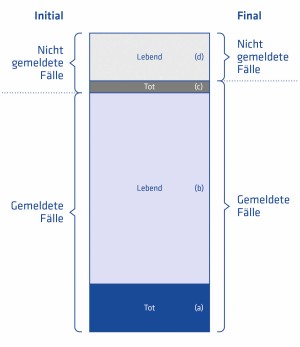
In Abb. 3 werden Krebsfälle unterteilt in zu Lebzeiten registrierte Fälle, die im Berichtsjahr noch leben (Anzahl b) oder gestorben sind (Anzahl a) sowie nicht registrierte Lebende (Anzahl d) und Verstorbene (Anzahl c). Die nicht registrierten Todesfälle (c) werden dem Krebsregister durch Einsicht in die Leichenschauscheine bekannt. Nimmt man an, dass von den nicht registrierten Fällen der gleiche Anteil verstorben ist wie von den Registrierten a: (a b), so kann die Zahl der lebenden, nicht registrierten Patienten (d) und damit auch die Gesamtzahl der erwarteten Krebsfälle gut abgeschätzt werden.
Das Hessische Krebsregister muss seine Daten jährlich dem Zentrum für Krebsregisterdaten (ZfKD) des Robert Koch-Instituts vorlegen, um u.a. das Kriterium der Vollzähligkeit überprüfen zu lassen. Dort werden die hessischen Daten mit einem durch kom-plexe Berechnungen (Stegmeier et al., 2019) erhaltenen Erwartungswert verglichen. Im Jahr 2017 wurde in Hessen das Kriterium der Vollzähligkeit (Registrierung von > 90 % der tatsächlichen vorhandenen Krebserkrankungen) erstmals erfüllt.
Abb. 3: DCI (Death certificate initiated)-Verfahren zur Abschätzung der Vollzähligkeit (adaptiert nach Parkin et al., 2009)
Finanzierung
Das Hessische Krebsregister wird im epidemiologischen Teil finanziert durch das Land Hessen, im klinischen Teil gemäß § 65c Abs. 2 SGB V zu 10 % durch das Land Hessen und zu 90 % durch die Krankenkassen. Die Krankenkassen zahlen einmalig für jede verarbeitete Meldung zur Neuerkrankung an einem Tumor eine fallbezogene Krebsregisterpauschale in Höhe von (aktuell) 141 Euro. Voraussetzung für die Finanzierung ist für die Krebsregister die Erfüllung von insgesamt 43 Förderkriterien, wozu u. a. das der Vollzähligkeit gehört.
Die Melder bekommen je nach Meldeanlass die in Tab. 1 aufgeführten Vergütungen. Ein Melder kann nur die Leistung abrechnen, die er selbst erbracht hat. So bekommt z. B. der Gastroenterologe für das von ihm endoskopisch diagnostizierte und gemeldete Zökumkarzinom 18 € vergütet, der Pathologe, der die histologische Diagnose gestellt und gemeldet hat, 4 €, der Viszeralchirurg, der es operiert und gemeldet hat, 5 € und der Onkologe, der den Beginn einer adjuvanten Chemotherapie meldet, 8 €.
Qualitätssicherung
Die Aktivitäten aller an der Krebsbekämpfung Beteiligten wirksamer aufeinander abzustimmen und ein zielorientiertes Vorgehen zu befördern, ist ein Ziel des Nationalen Krebsplans, den das Bundesgesundheitsministerium gemeinsam mit der Deutschen Krebsgesellschaft, der Deutschen Krebshilfe und der Arbeitsgemeinschaft Deutscher Tumorzentren 2008 ins Leben gerufen hat.
Im Handlungsfeld 2 „Weiterentwicklung der onkologischen Versorgungsstruktur und der Qualitätssicherung“ findet sich das Ziel 8: „Es existiert eine aussagekräftige onkologische Qualitätsberichterstattung für Leistungserbringer, Entscheidungsträger und Patienten.“ Mit dieser Aufgabe der Qualitätssicherung wurden die klinischen Krebsregister betraut.
So ist z. B. die Registrierung von Intervallkarzinomen ein wichtiger Indikator für die Effektivität von Screeningverfahren wie der Vorsorgekoloskopie und dem Mammographiescreening.
Bei der Beurteilung der Qualität der Krebsregistrierung spielen vier Schlüsselaspekte eine Rolle (Bray et al., 2009):
- Validität (Gültigkeit) Die „Richtigkeit“ der Daten ist abhängig einerseits von der Genauigkeit der Datenerhebung, andererseits vom Sachverstand bei ihrer Beurteilung und Kodierung. Die Validität beinhaltet u. a. die Übereinstimmung gemeldeter und kodierter Information und die Reproduzierbarkeit in der Herstellung der Registerdaten. Es kann in Audits überprüft werden, inwieweit verschiedene Dokumentare mit einem vorgegebenen Probe-Datensatz zu gleichen Ergebnissen/Registereinträgen kommen. Geprüft wird auch die Zuverlässigkeit, mit der Dokumentare vorgegebene Regelwerke verstehen und anwenden. Der Anteil histologisch gesicherter Tumore stellt ein weiteres Validitätskriterium dar.
- Komparabilität (Vergleichbarkeit) Die Vergleichbarkeit ist nur gegeben, wenn die Meldungen klaren Definitionen unterliegen und ihre Kodierung standardisiert ist. Überprüft wird sie, indem ihre Vereinbarkeit mit internationalen Verfahrensstandards festgestellt wird. Beispiele dafür sind: Welches Tumorklassifikationssystem wird benutzt? Wann ist ein Tumor als Zweittumor zu werten, wann als Rezidiv, wann als Metastase eines Ersttumors?
- Aktualität Nur durch aktuelle Übermittlung und Verarbeitung von Tumordaten lassen sich andere Qualitätsindikatoren wie Genauigkeit und Vollzähligkeit erreichen. Die Latenz zwischen Diagnose und Verwertbarkeit der Daten im Register teilt sich auf in das Intervall von der Diagnose bis zum Dateneingang im Register und das Bearbeitungsintervall. Nach den US-amerikanischen Centers of Disease Control (CDC) ist ein Register dann aktuell, wenn es Daten 24 Monate nach dem Ende des Berichtsjahres mit einer Vollzähligkeit > 95 % zur Verfügung stellen kann. Das seit 1953 betriebene norwegische Krebsregister ist in der Lage, schon zum Ende des auf das Berichtsjahr folgenden Jahres Auswertungen zu liefern (Larsen et al., 2009).
- Vollständigkeit Nur wenn die Behandlungsinformationen zu einer Krebserkrankung vollständig erfasst sind und somit das Tumorgeschehen eines Patienten vollständig abgebildet ist, können aussagekräftige Werte für z. B. Inzidenz und Überlebensrate ermittelt und Behandlungsverfahren miteinander verglichen werden.
Datenschutz
Es können drei Krebsregistermodelle unterschieden werden, die auf unterschiedliche Art und Weise die Aspekte des Datenschutzes berücksichtigen:
- Informationsmodell: Der Patient muss über sein Widerspruchsrecht aufgeklärt werden. Einer schriftlichen Einwilligung für die Tumormeldung bedarf es nicht (so verwirklicht im Hessischen Krebsregister).
- Melderechtsmodell: Jeder Arzt darf an das Krebsregister melden, ohne dass der Patient über die Meldung unterrichtet werden muss.
- Verschlüsselungsmodell: Jeder Arzt darf an das Krebsregister melden, wobei die personenidentifizierenden Angaben lediglich pseudonymisiert verarbeitet werden dürfen. Bei dieser Form der Krebsregistrierung kann weiter differenziert werden:
- Zentrale Verschlüsselung: Die Meldungen werden an das Krebsregister übermittelt und dort zentral verschlüsselt.
- Dezentrale Verschlüsselung: Die Verschlüsselung wird vom Melder (z. B. Arzt) direkt vorgenommen und die Meldung bereits pseudonymisiert an das Krebsregister übermittelt.
Beim Melderechtsmodell, welches die international anerkannte Form der Registrierung von Krebsmeldungen darstellt, werden die ärztliche Schweigepflicht und der Datenschutz am stärksten belastet.
Nutzung von Krebsregisterdaten
Die Krebsregister sollen nach dem Krebsfrüherkennungs- und -register-Gesetz (KFRG) eine Verbesserung der onkologischen Versorgungsqualität herbeiführen.
Die Nutzung der Krebsregister umfasst:
- Gesundheitsberichterstattung: Das Hessische Krebsregister veröffentlicht seine Ergebnisse im Report „Krebs in Hessen“. In Deutschland werden die Daten der Landeskrebsregister durch das am Robert Koch-Institut angesiedelte Zentrum für Krebsregisterdaten (ZfKD) zu einer Bundesstatistik zusammengefasst. In Europa übernimmt das European Network of Cancer Registries (ENCR), weltweit die zur WHO gehörende International Agency for Research on Cancer (IARC) diese Aufgabe.
- Unterstützung von Tumorkonferenzen: So könnte z. B. mit Hilfe des Krebsregisters der Kontakt zwischen den Behandlern einer seltenen Tumorentität zum Erfahrungsaustausch vermittelt werden.
- Aggregierte Rückmeldungen an die Leistungserbringer u. a. zum Zwecke der Selbst- bzw. Erfolgskontrolle. Auch vergleichende Rückmeldungen im Sinne eines „Benchmarkings“ sind möglich.
- Durchführung von Qualitätskonferenzen: Im Rahmen der Konferenzen wird evaluiert, inwieweit Leitlinienempfehlungen umgesetzt werden. Es werden Auswertungen zu gültigen Qualitätsindikatoren vorgestellt und diskutiert. Erforderliche Maßnahmen zur Qualitätsverbesserung werden initiiert.
- Zusammenarbeit mit onkologischen Zentren: Ein onkologisches Zentrum muss im Rahmen seiner Zertifizierung die Zusammenarbeit mit einem Krebsregister nachweisen.
- Evaluation von Krebsfrüherkennungsmaßnahmen mittels Kohortenabgleich So wird z. B. durch Abgleich der am Mammographiescreening teilnehmenden Frauen mit dem Datenbestand des Krebsregisters die Rate an Intervallkarzinomen festgestellt (Urbschat et al., 2014).
- Bereitstellung von Daten für die onkologische Forschung: Die Krebsregister-Daten können insbesondere im Rahmen der epidemiologischen und Versorgungsforschung genutzt werden. Klinische Krebsregisterdaten können z. B. genutzt werden, um im Rahmen von Phase III-Studien die Wirksamkeit neuer Therapie-Optionen zu analysieren und Nutzen-Bewertungen abzugeben
Das Krebsregister kann aggregierte (d. h. nach Merkmalen wie z. B. Alter, Geschlecht, Zeitraum zusammengefasste Daten) oder Einzelfalldaten zur Verfügung stellen. Sofern in der geplanten Studie personenbezogene Daten verarbeitet werden sollen, sind umfangreiche Voraussetzungen zu erfüllen (u. a. Bestätigung der „good epidemiological practice“, Votum der Ethikkommission, ggf. Genehmigung durch das zuständige Ministerium, Stellungnahme durch den Datenschutzbeauftragten).
Anmeldung Hessisches Krebsregister: Über den „Anmeldeservice Hessisches Krebsregister“ im Mitgliederportal der Landesärztekammer Hessen können sich Ärztinnen und Ärzte in Hessen schnell und einfach als Melderin bzw. Melder registrieren: Mitgliederportal → Services → Formulare → Anmeldeservice Hessisches Krebsregister.
Tab. 1: Derzeit gültige Vergütungssätze des Hessischen Krebsregisters | |||
Meldeanlass | Vergütung pro Meldung | ||
Erwachsene | Minderjährige (Leistungsdatum vor dem 24.12.2019) | Minderjährige (Leistungsdatum ab dem 24.12.2019) | |
Diagnosestellung | 18,00 Euro | 5,00 Euro | 18,00 Euro |
Zahnärztliche Diagnose | 15,00 Euro | | |
Verlaufsdaten | 8,00 Euro | 3,00 Euro | 5,00 Euro |
Therapie- und Abschlussdaten | 5,00 Euro | 3,00 Euro | 5,00 Euro |
Pathologische Diagnosesicherung | 4,00 Euro | 3,00 Euro | 4,00 Euro |
Multiple Choice-Fragen
Die Multiple Choice-Fragen zu dem Artikel „Hessisches Krebsregister: Klinisch-epidemiologische Krebsregistrierung in Hessen“ von Dr. med. Gunther Rexroth, Martin Rapp und Vera Reinhard finden Sie am Ende dieser Seite unter „Artikel herunterladen“ in der PDF-Version dieses Artikels und im Mitglieder-Portal unter https://portal.laekh.de. Die Teilnahme zur Erlangung von Fortbildungspunkten ist ausschließlich online über das Mitglieder-Portal vom 25. Januar 2022 bis 24. Juli 2022 möglich. Die Fortbildung ist mit zwei Punkten zertifiziert. Mit Absenden des Fragebogens bestätigen Sie, dass Sie dieses CME-Modul nicht bereits an anderer Stelle absolviert haben. Dieser Artikel hat ein Peer-Review-Verfahren durchlaufen. Nach Angaben der Autoren sind die Inhalte des Artikels produkt- und/oder dienstleistungsneutral, es bestehen keine Interessenkonflikte.
Dr. med. Gunther Rexroth, Ärztlicher Leiter, Martin Rapp, Organisatorischer Leiter, Vera Reinhard, Wissenschaftliche Referentin
alle: Vertrauensstelle des Hessischen Krebsregisters bei der Landesärztekammer Hessen
Die Literaturhinweise finden Sie am Ende dieser Seite unter „Artikel herunterladen“ in der PDF-Version dieses Artikels.