VNR: 2760602020095090004
Dr. med. Christian Reinhardt, Prof. Dr. med. Stefan Andreas, Dr. med. Peter Hammerl
Die Tuberkulose ist weltweit unverändert noch vor AIDS und Malaria die häufigste tödlich verlaufende Infektionserkrankung. Statistisch gesehen sterben jede Minute drei Menschen an den Folgen der Erkrankung. Infolge der Migration in jüngerer Zeit ist die Zahl der Tuberkuloseerkrankungen in Deutschland erstmals wieder angestiegen. Angesichts eines Anstiegs der Tuberkuloseinzidenz um 27 % von 2014 auf 2015, entsprechend dem Niveau von 2005, ist die Tuberkulose wieder ins Bewusstsein der Ärzte und der breiteren Öffentlichkeit gerückt.
Die Befürchtung anhaltend erhöhter Neuerkrankungsraten hat sich in der Folge nicht bestätigt. Ausgehend von der maximalen Neuerkrankungsrate von 7,2/100.000 Einwohner im Jahr 2016 ist eine stete Abnahme in den Folgejahren bis auf unter 6/100.000 im Jahr 2019 zu verzeichnen. Dies entspricht dem Stand aus dem Jahr 2005. Die Erkrankung ist in Deutschland weiterhin sehr selten.
Am häufigsten ist die Lungentuberkulose, weshalb die Behandlung der Erkrankung schon immer in der Hand der Pneumologen lag. Die offene Lungentuberkulose ist infektiös, daher sind spezielle Isolationsmaßnahmen und Umgebungsuntersuchungen zur Erfassung der Ausbreitung der Erkrankung erforderlich. Die Behandlung richtet sich nach der Resistenzlage, der Ausdehnung der Erkrankung und dem befallenen Organsystem. An erster Stelle steht bei Erwachsenen die antituberkulöse medikamentöse Mehrfachtherapie mit initial mindestens vier verschiedenen Medikamenten. Wenige Sonderformen machen andere therapeutische Maßnahmen erforderlich. Die Erkrankung und die Verweigerung bzw. der Abbruch der Behandlung sowie der Tod an Tuberkulose sind gemäß § 6 IfSG bei der zuständigen Behörde meldepflichtig, auch wenn ein bakteriologischer Nachweis nicht vorliegt.
Epidemiologie
Seit der Gründung der Bundesrepublik sind die Inzidenzraten kontinuierlich von initial 277/100.000 (137.721 Fälle!) auf unter 7/100.000 ab dem Jahr 2006 zurückgegangen. 2015 wurde mit 5.837 Meldungen (7,1/100.000) diese Marke erstmals wieder überschritten [1]. Die Meldezahlen für 2017 zeigen mit 5542 Neuerkrankungen bzw. 5.429 Neuerkrankungen für 2018 bereits wieder eine rückläufige Tendenz. Knapp 70 % der Erkrankten haben einen Migrationshintergrund. Im Jahr 2016 wurden 25 % der gemeldeten Tuberkulosen durch Maßnahmen der aktiven Fallfindung (Röntgenuntersuchungen vor Unterbringung in Gemeinschaftsunterkünften, Umgebungsuntersuchungen, Überwachung gesunder Befundträger, Röntgenscreening in Justizvollzugsanstalten) entdeckt. Dieser Anteil lag im Jahr 2006 bei 13,8 %. Weltweit ist die Zahl der Tuberkuloseneuerkrankungen leider unverändert auf hohem Niveau. Der WHO-Report 2019 spricht von zehn Millionen Neuerkrankungen im Jahr 2018.
Erreger
Die Tuberkulose wird in Deutschland zu 97 % durch Mycobacterium (M.) tuberculosis verursacht. Infektionen durch M. bovis, africanum, microti, canetti oder pinnipedii sind äußerst selten. Diese obligat pathogenen Mykobakterien werden unter dem Begriff M. tuberculosis-Komplex (MTB-Komplex) zusammengefasst und jeder plausible Erregernachweis ist behandlungspflichtig. Die Mykobakterien zeichnen sich durch ihr langsames Wachstum aus, dies erfordert lange Kulturzeiten (bis zu acht Wochen) auf Spezialmedien. Unter Ausnutzung der Säureresistenz der Mycobacterien sind sie nur durch besondere Färbeverfahren (Ziehl-Neelsen-, Auramin- oder Kinyoun-Färbung) nachweisbar, daher die Bezeichnung „säurefeste Stäbchen“.
Es treten Resistenzen gegen nahezu alle verwendeten Medikamente auf. Bei M. bovis liegt eine natürliche Pyrazinamid-Resistenz vor.
Klinisches Bild
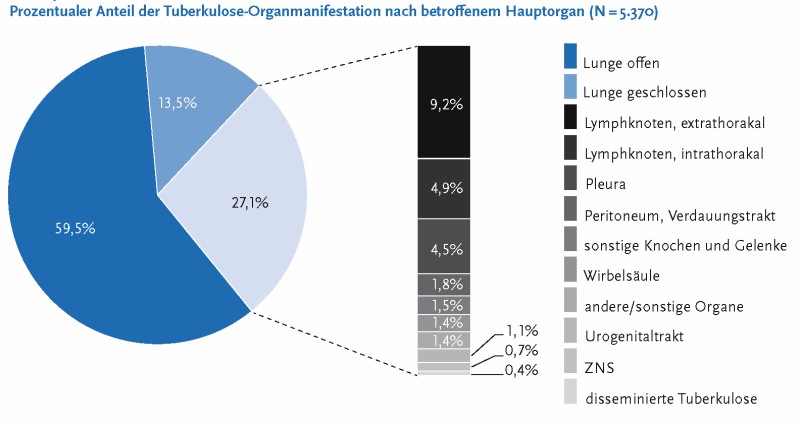
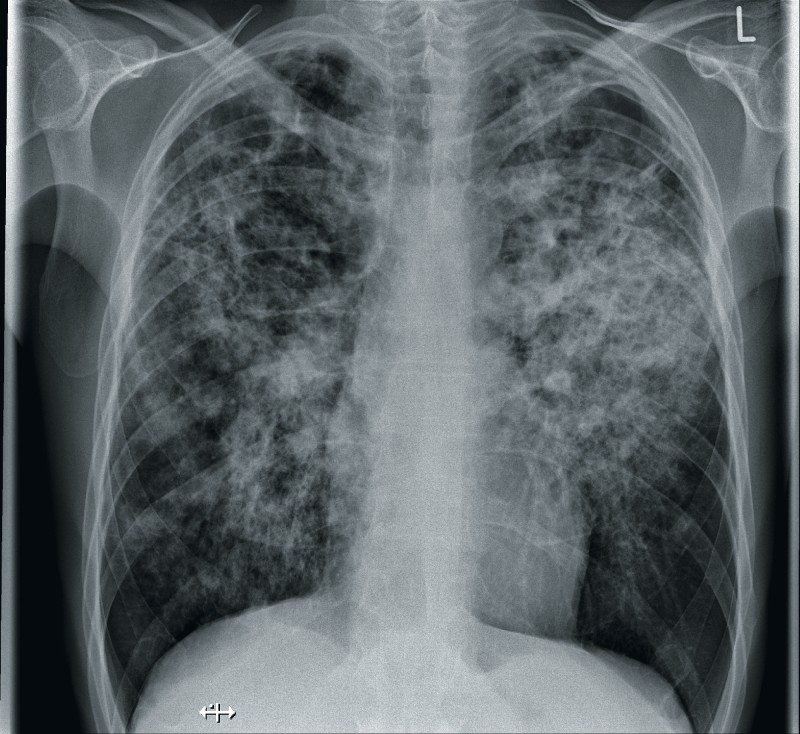
Die Tuberkulose zählt zu den konsumierenden Erkrankungen. Da die Primärinfektion per inhalationem erfolgt, ist die Lunge das am häufigsten betroffene Organ (Abb. 1).
Es gibt aber auch oligo- oder vollkommen asymptomatische Verläufe bei bereits fortgeschrittener Erkrankung, dann ist die Diagnosefindung äußerst erschwert. Die extrapulmonalen Erkrankungsformen werden durch die extrathorakale (wesentlich häufiger, meist cervikal) und intrathorakale Lymphknotentuberkulose sowie die Pleuritis tuberculosa angeführt. Der Lymphknotenbefall ist durch über Wochen zunehmende Lymphknotenschwellungen meist ohne Druckdolenz charakterisiert. In einigen Fällen kommt es zur spontanen Eröffnung der Läsionen. Typischerweise heilen die Wunden nach Biopsien oder Lymphknotenexstirpation ohne eine antituberkulöse medikamentöse Therapie nicht ab und es kommt zur Fistelbildung.
Alle weiteren Formen der Tuberkulose sind selten. Bei unklaren Abszessen, Granulomen, fistelnden Wunden, Aszites, Osteolysen oder einer Spondylodiszitis sollte eine Tuberkulose in Betracht gezogen werden. Nur wer daran denkt, kann die Diagnose auch sichern.
Diagnostik
Radiologische Diagnostik
Bei Verdacht auf eine Tuberkulose steht die Röntgenaufnahme der Thoraxorgane an erster Stelle.
Auf eine Lungentuberkulose hinweisende radiologische Zeichen sind:
- Kavernenbildung
- Fleckige infiltrative Veränderungen im Bereich der Oberlappen, des Mittellappens oder der Lingula sowie der apikalen Unterlappen
- Hiläre oder mediastinale Lymphknotenschwellungen
- Intrapulmonale, pleurale oder Lymphknotenverkalkungen
- Schrumpfungen der Lunge
- Pleuraerguss
- Mittellappenatelektase
- Kleinknotige, miliare Veränderungen
In den vergangenen Jahren werden aber zunehmend atypische radiologische Veränderungen beobachtet, so dass eine Tuberkulose insbesondere bei komplizierten oder therapieresistenten Befunden immer in Betracht gezogen werden sollte, speziell dann, wenn besondere Risikofaktoren für die Erkrankung vorliegen. Eine Kaverne ist bis zum Beweis des Gegenteils stets verdächtig auf eine tuberkulöse Genese. Auch bei extrapulmonaler Manifestation sind nicht selten pulmonale oder mediastinale Veränderungen zu finden und eine Röntgenaufnahme des Thorax obligat.
Da die Diagnose aus der Trias „Klinik, radiologischer Befund und Erregernachweis im Sputum“ gesichert werden kann, ist die Computertomographie des Thorax im Rahmen der Primärdiagnostik meist entbehrlich. Sie bleibt speziellen Fragestellungen vorbehalten.
Mikrobiologische Diagnostik
Hier steht nach wie vor die Sputummikroskopie an erster Stelle. Wird kein Sputum produziert, stellt die Untersuchung von Magensaft eine gute Alternative dar. Die Mikroskopie ist schnell und kostengünstig. Die Nachweisgrenze im Sputum liegt bei etwa 5.000 Bakterien pro ml, die Sensitivität in Abhängigkeit von der Methode bei 20–70 % [2]. Allerdings ist eine Unterscheidung zwischen toten und lebendigen Mykobakterien nicht möglich. Säurefeste Stäbchen lassen sich auch in Gewebeproben oder anderen Materialien anfärben. Nicht nur die Erreger des MTB-Komplexes sondern auch nichttuberkulöse Mykobakterien oder Nocardien lassen sich durch die Spezialfärbungen nachweisen, so dass nicht jeder positive Befund mit einer Tuberkulose gleichzusetzen ist.
Bei bis zu 70 % der Erkrankten können im Sputum säurefeste Stäbchen nachgewiesen werden. Dabei ist der Sputumbefund abhängig vom Lebensalter. Aufgrund des geringen Hustenstoßes finden sich bei Kindern unter 14 Jahren lediglich bei ca. 25 %, bei alten Menschen > 79 Jahren bei ca. 45 % pathologische Sputumbefunde. Kleinkinder scheiden fast nie Erreger über den Husten aus [1].
Der zusätzliche Einsatz von Nukleinsäure-Amplifikations-Techniken (zum Beispiel PCR) hilft bei der Erregeridentifikation und liefert abhängig von der eingesetzten Sonde Aussagen zur Resistenzlage. Das Ergebnis steht nach wenigen Stunden zur Verfügung. Sensitivität und Spezifität sind höher als bei der Mikroskopie und liegen bei mikroskopisch positiven Materialien bei nahezu 100 %, so dass eine negative PCR bei positiver Mikroskopie eine Tuberkulose praktisch ausschließt. Bei fehlendem mikroskopischen Nachweis von säurefesten Stäbchen im Untersuchungsmaterial ist die Sensitivität der PCR allerdings auch eingeschränkt und liegt hier zwischen 80–90 %; in formalinfixiertem Gewebe ist sie viel niedriger [3, 4], so dass in diesen Fällen eine negative PCR eine Tuberkulose niemals ausschließt!
Goldstandard bleibt der kulturelle Erregernachweis. Hierzu werden die Materialien nach DIN aufgearbeitet und auf verschiedene Kulturmedien (ein Flüssig- und zwei Festkulturmedien) beimpft. Die Bebrütung erfolgt für 56 Tage. Ein positives Ergebnis ist je nach Ausfall der Mikroskopie nach 1–8 Wochen zu erwarten. Erst der positive Kulturbefund beweist die Vitalität des Erregers und macht in-vitro-Resistenztestungen möglich. Die PCR-Technik hingegen ist bei der Frage der Vitalität genauso wenig hilfreich wie die Mikroskopie, da auch tote Erreger genetisch erfasst werden und die PCR somit noch Jahre nach Ausheilung der Tuberkulose positiv bleiben kann.
Die Kultur ist nur aus nativem Material (Sputum, Bronchialsekret, Gewebe, Pleuraerguss, Aszites, Urin, Fistelsekret etc.) möglich. Fixation in Formalin verhindert das Wachstum der Erreger und macht eine Anzucht unmöglich. Wenn Gewebe zur Tbc-Diagnostik gewonnen werden soll, muss der Operateur daher explizit auf diesen Sachverhalt hingewiesen werden!
Grundsätzlich schließt keines der mikrobiologischen Verfahren eine aktive Tuberkulose sicher aus. Immerhin sind gut 25 % der gemeldeten Fälle mikrobiologisch nicht gesichert [1].
Die Resistenzprüfung kann kulturell (phänotypisch nach der Proportionalmethode) oder genotypisch mit Sonden erfolgen. Letztgenannte ist allerdings wenigen Speziallaboratorien vorbehalten. Bei stark bakteriell verunreinigten Kulturen kann die genotypische Resistenzbestimmung richtungsweisend sein.
Immunologische Tests
Die immunologischen Testverfahren beruhen auf dem Nachweis einer zellulären Typ-IV-Reaktion auf Tuberkulin oder der in-vitro Reaktion von T-Lymphozyten auf ausgewählte Antigene von M. tuberculosis. Eine sichere Unterscheidung zwischen aktiver Erkrankung und latenter Tuberkuloseinfektion ist mit diesen Verfahren nicht möglich. Sie dienen in erster Linie dem Nachweis einer latenten Tuberkuloseinfektion. Für die Diagnose der aktiven Erkrankung spielen sie nur eine untergeordnete Rolle.
Mittlerweile wurden die Hauttests weitgehend von den Interferontests abgelöst.
Tuberkulinhauttest (THT)
Zur Hauttestung steht nur noch ein Tuberkulinpräparat (PPD23 purified protein derivate des Statens Serum Institut, Kopenhagen) zur Verfügung. Es werden mit dünner Kanüle 2 TE (Tuberkulin-Units), entsprechend 0,1 ml streng intradermal an der Beugeseite des Unterarms injiziert. Die Immunreaktion wird nach 72 Stunden abgelesen, was einen zweiten Patientenkontakt erforderlich macht. Von diagnostischer Relevanz ist nicht die Rötung sondern der Durchmesser der Schwellung. Die Interpretation ist untersucherabhängig und bezieht das Erkrankungsrisiko mit ein [5]. Insbesondere nach einer wenige Jahre zurückliegenden BCG-Impfung kann der THT falsch positiv ausfallen [6].
Interferon-Gamma-Release-Assay (IGRA)
Durch den IGRA wird eine Immunreaktion auf Antigenbestandteile von M. tuberculosis nachgewiesen. Hierzu wird Vollblut der Patienten mit Allergenbestandteilen von Mykobakterien inkubiert. Nach Kontakt mit dem Erreger werden T-Lymphozyten aktiviert, die Interferon-ɣ freisetzen. Der Nachweis ist quantitativ mit verschiedenen Methoden möglich. Am Markt sind zwei Testsysteme erhältlich.
Der Vorteil der IGRAs beruht auf der deutlich höheren Spezifität und der einfachen Handhabung im Alltag. Bei vorausgegangener BCG-Impfung bleibt der Test negativ, so dass positive Reaktionen auf einen stattgehabten Kontakt mit Erregern aus dem MTB-Komplex hinweisen. Falsch positive Befunde treten allerdings auch bei den IGRAs auf. Problematisch ist die Interpretation von Grenzbefunden. Der Test kann genauso wenig wie der Hauttest zwischen einer behandlungsbedürftigen Erkrankung und einer latenten Tuberkuloseinfektion unterscheiden und sollte daher allenfalls ergänzend zur Diagnose der aktiven Erkrankung verwendet werden [7]. Die Sensitivität der IGRAs liegt bei etwa 80% [8]. Die Aussagekraft ist insbesondere bei Immunsupprimierten und Kindern unter fünf Jahren eingeschränkt.
Ein negativer IGRA schließt eine aktive Tuberkulose nie mit Sicherheit aus, ein positiver beweist sie nicht. Da nach Tuberkuloseexposition eine definitive immunologische Reaktion erst nach acht Wochen zu erwarten ist, sollte z. B. bei Umgebungsuntersuchungen so lange mit dem Test gewartet werden. Für Kinder und Jugendliche unter 15 Jahren gelten andere Regeln.
Weder der Haut- noch IGRA-Test werden in der aktuellen Leitlinie [5] zur Primärdiagnostik empfohlen. Sie haben aber einen wichtigen Stellenwert im Rahmen der Infektionsprävention durch den öffentlichen Gesundheitsdienst und als Screeningmethode vor dem Einsatz diverser Biologicals (zum Beispiel Infliximab bei rheumatoider Arthritis).
Latente Tuberkulose
Nicht jeder Nachweis einer Immunreaktion auf mykobakterielle Proteine im THT oder IGRA ist mit einer aktiven Tuberkulose gleichzusetzen. Lässt sich trotz sorgfältiger Diagnostik keine aktive Erkrankung nachweisen, spricht man von einer latenten Tuberkulose. Die Infizierten sind klinisch gesund und nicht ansteckend. Es wird davon ausgegangen, dass eine aktive Erkrankung durch eine erfolgreiche Immunabwehr verhindert werden konnte ohne dass aber alle Erreger komplett abgetötet wurden. Die Persistenz der Bakterien birgt die Gefahr einer Aktivierung, wenn die immunologische Kontrolle durch Erkrankungen oder Medikamente, welche die Immunkompetenz negativ beeinflussen verloren geht. Schätzungen zufolge findet man bei ca. ¼ der Weltbevölkerung einen positiven IGRA oder THT [9]. Das Lebenszeitrisiko für die Entwicklung einer aktiven aus einer latenten Tuberkulose beträgt etwa 5–10 %.
Bei Nachweis einer latenten Tuberkulose ist nur bei hohem Risiko für die Entwicklung einer aktiven Tuberkulose eine Therapie erforderlich. Prinzipiell sollte eine Untersuchung auf eine latente Tuberkuloseinfektion nur erfolgen, wenn ein erhöhtes Risiko für eine Infektion besteht wie etwa bei Kontaktpersonen zu einem Patienten mit ansteckender Lungentuberkulose oder bei gesteigertem Reaktivierungsrisiko etwa unter immunsuppressiver Therapie.
Da nur von einer geringen Anzahl von vitalen Erregern auszugehen ist, ist eine Therapie mit einem oder zwei Medikamenten ausreichend. Bevorzugt wird eine Behandlung mit Rifampicin über vier Monate oder eine Kombinationstherapie mit Isoniazid und Rifampicin über drei Monate. Die früher bevorzugte Monotherapie mit Isoniazid über neun Monate führt wegen der langen Einnahmedauer häufig zu Behandlungsabbrüchen und wird daher zunehmend weniger eingesetzt. Bei Resistenzen oder Unverträglichkeiten wird die Chemoprävention kompliziert und muss in die Hand von mit der Therapie der Tuberkulose vertrauten Ärzte gegeben werden. In Tab. 1 sind Risikogruppen aufgeführt, bei denen eine Chemoprävention im Falle einer latenten Tuberkulose erwogen werden sollte. Auch im Falle der Chemoprävention muss das Risiko von Nebenwirkungen der Therapie berücksichtigt werden.
Tab. 1: Risikogruppen mit erhöhtem Risiko für die Ausbildung einer aktiven Tuberkulose bei nachgewiesener latenter Tuberkulose modifiziert nach [7] |
Enger Kontakt zu Patienten mit nachgewiesener aktiver Tuberkulose |
Vor oder unter Therapie mit TNF-Alpha-Blockern und anderen Biologicals |
HIV-Infektion |
Schwerwiegende Grunderkrankung: Diabetes mellitus, Lymphome, Leukämie, Kopf-, Halstumoren |
Silikose |
Schwangere, bei kürzlich zurückliegender Infektion oder Immunsuppression |
Vor oder nach Organ- oder hämatologischer Transplantation |
Dialysepatienten |
i.v.-Drogenabhängigkeit |
Herkunft aus Risikogebieten mit hoher Tuberkuloseinzidenz, Obdachlose, Personen in Justizvollzugsanstalten, Lungenabteilungen oder Gesundheitswesen |
Kinder unter vier Jahren |
Unter Chemoprophylaxe versteht man die Gabe von Tuberkulosemedikamenten zum frühestmöglichen Zeitpunkt nach Exposition, wenn sich noch keine immunologische Reaktion in Form eines positiven Tuberkulinhauttests oder eines positiven IGRA nachweisen lässt. Sie soll das Angehen einer Neuinfektion bei Risikopersonen (z. B. Kinder unter fünf Jahren und Patienten unter Immunsuppression) verhindern und erfolgt mit einer INH-Monotherapie. Vor dieser Maßnahme muss radiologisch eine aktive Erkrankung ausgeschlossen werden. Ist nach acht Wochen Therapie der IGRA oder THT negativ, kann die Prophylaxe beendet werden. Bei positivem Ergebnis wird die Therapie als Prävention über insgesamt neun Monate fortgeführt.
Diagnosestellung
Oberstes Ziel der Diagnostik sind die Sicherung der Diagnose und der definitive Keimnachweis, damit unnötige Behandlungen mit potenziell nebenwirkungsträchtigen Medikamenten und Fehldiagnosen vermieden werden können. Das Spektrum der Differenzialdiagnosen ist breit (siehe Tab. 2). Die Diagnose gilt als zweifelsfrei gesichert, wenn bei plausiblen klinischen, radiologischen oder histo- bzw. zytopathologischen Befunden mittels PCR oder Kultur der Erregernachweis gelingt. Die Gewinnung von geeignetem Material für die mikrobiologische Diagnostik und Nachweis etwa vorliegender Resistenzen steht daher an oberster Stelle. Bei ca. 25 % der jährlich gemeldeten Erkrankungen gelingt kein Erregernachweis. Hier wird die Diagnose aus der Zusammenschau der erhobenen Befunde, dem Ausschluss von Differentialdiagnosen und anhand des Ansprechens auf eine antituberkulöse Therapie gestellt.
Tab. 2: Mögliche Differentialdiagnosen thorakaler Tuberkuloseformen (ohne Anspruch auf Vollständigkeit) | |
Organsystem | Mögliche Diagnosen |
Lunge | Bronchialkarzinom |
Gewöhnliche Pneumonie | |
Vaskulitis | |
Cryptogen organisierende Pneumonie | |
Sarkoidose | |
Lymphknoten | Lymphome |
Sarkoidose | |
Infektiöse Lymphadenitis durch andere Erreger | |
Pleura | Bronchialkarzinom |
Mesotheliom | |
Pleurale Metastasierung extrathorakaler Malignome | |
Parainfektiöser Pleuraerguss | |
Pleuraerguss bei rheumatischer Grunderkrankung | |
In mehr als 90 % der Fälle erfolgen die Diagnosesicherung und die Einleitung einer Therapie unter stationären Bedingungen. Die primäre Bronchoskopie ist nur bei negativer Sputummikroskopie indiziert, zumal sie bei Erregerausscheidern ein erhebliches Infektionsrisiko für den Untersucher und das Endoskopieteam darstellt. Mittels Spülung, bronchoalveolärer Lavage (BAL) oder transbronchialer Biopsie (TBB) kann geeignetes Material zur Diagnostik gewonnen werden. Intrathorakale Lymphknoten können mittels endobronchialem Ultraschall (EBUS) gezielt punktiert werden. Bei den extrapulmonalen Formen ist in der Regel eine Sonographie- oder CT-gesteuerte Biopsie zur Materialgewinnung für die mikrobiologische bzw. pathologisch-histologische Untersuchung erforderlich, bei der Meningitis tuberculosa oder zerebralen Tuberkulose eine Liquorpunktion. Bei der Urogenitaltuberkulose sollten Urin, Ejakulat oder Menstrualblut zur Kultur asserviert werden. PCR und Mikroskopie aus Aszites und Pleuraergüssen bleiben meist negativ, da es sich hierbei um ein paucibacilläres Material handelt. Sie sollten aber dennoch untersucht werden. Ergiebiger ist die Diagnostik aus einer Pleurabiopsie, die perkutan oder im Rahmen einer Thorakoskopie gewonnen werden kann. Zur Diagnose der Abdominaltuberkulose ist häufig eine Laparoskopie notwendig.
Therapie
Im Erwachsenenalter ist die medikamentöse Mehrfachtherapie aus initial mindestens vier verschiedenen, gegen Mykobakterien wirksamen Antibiotika Standard. Die Dreifach-Therapie ist obsolet. Bei der unkomplizierten Tuberkulose ohne zu erwartende Resistenzen werden Rifampicin (RMP), Isoniazid (INH), Ethambutol (EMB) und Pyrazinamid (PZA) eingesetzt. An die zweimonatige Initialphase mit einer vierfach-Therapie schließt sich die viermonatige Kontinuitätsphase mit einer zweifach-Therapie (RMP, INH) an, woraus sich eine Gesamttherapiedauer von sechs Monaten ergibt (siehe Tab. 3).
Tab. 3: Dosierung der Standardtherapie, nach [7] | ||||
Substanz | Dosis1 (mg/kg KG) | Dosisbereich (mg/kg KG) | Minimal- und Maximaldosis (mg) | Dosis bei 70 kg Körpergewicht (mg) |
Isoniazid (INH) | 5 | 4–6 | 200/ 300 | 300 |
Rifampicin (RMP) | 10 | 8–12 | 450/ 600 | 600 |
Pyrazinamid (PZA) | 25 | 20–30 | 1500/ 2500 | 1750 |
Ethambutol (EMB)2 | 15 | 15–20 | 800/ 1600 | 1200 |
1 Dosisanpassung bei steigendem Körpergewicht im Heilungsverlauf beachten! 2 Optimale Dosis nicht bekannt, Okkuläre Nebenwirkungen in dieser Dosierung seltener. | ||||
Bei den komplizierten Formen der Tuberkulose mit gesicherten oder erwarteten Resistenzen, ausgedehnter Erkrankung (z. B. Kavernen, lange Zeit bis zur Sputumkonversion), Knochen-, Gelenk oder ZNS-Befall ändern sich Medikamentenkombination und Therapiedauer. In besonderen Fällen ist der zusätzliche Einsatz von Glucocorticoiden oder operativen Maßnahmen indiziert [7]. Die Standardmedikamente sollten morgens nüchtern eine halbe Stunde vor dem Frühstück und zumindest in der Klinik unter Aufsicht eingenommen werden.
Die aktuelle Leitlinie [7] empfiehlt bei einigen Monoresistenzen den Ersatz des unwirksamen Präparates durch eines der beiden Fluorchinolone Moxifloxacin oder Levofloxacin. Dabei verlängert sich die Therapiedauer auf bis zu 20 Monate. Andere Fluorchinolone sollten nicht mehr verwendet werden. Patienten mit einer RMP-Resistenz werden wie eine multiresistente Tuberkulose (MDR) behandelt.
Die Therapie von Mehrfach-, Multi- oder extensiv-resistenten Tuberkulosen ist komplex, die Patienten sollten Expertenzentren zugewiesen werden. Im Jahr 2018 ließ in Deutschland bei 13 % der gemeldeten Tuberkulosefälle mit bekannter Resistenzlage mindestens eine Resistenz nachweisen, eine Multiresistenz fand sich bei 3,1 % – siehe Tab. 4, [1].
Tab. 4: Definition der Resistenzbildung bei Tuberkulose, nach [7] | |
Monoresistenz | Resistenz gegen eines der Standardmedikamente |
Polyresistenz | Resistenz gegen mehr als ein Standardmedikament, jedoch nicht gleichzeitig gegen INH und RMP |
Multiresistenz (MDR) | Resistenz gegen mindestens INH und RMP |
Prä-extensive Resistenz (preXDR) | MDR plus Resistenz gegenüber mindestens einem Fluorchinolon oder einem der injizierbaren Medikamente (Amikacin, Capreomycin und Kanamycin) |
Extensive Resistenz (XDR) | MDR plus Resistenz gegenüber mindestens einem Fluor- chinolon und einem der injizierbaren Medikamente (Amikacin, Capreomycin und Kanamycin) |
Risikofaktoren für Resistenzen
- Eine mindestens vierwöchige Tuberkulosetherapie in der Vergangenheit mit oder ohne Unterbrechung,
- Kontakt zu einer Person mit einer resistenten Tuberkulose,
- Herkunft aus einem Hochrisikogebiet, insbesondere ehemalige Staaten der UdSSR.
Mittlerweile erlauben die molekularbiologischen Methoden eine zeitnahe valide Aussage zur Resistenzlage. Mittels PCR können dabei nicht nur die Diagnose der Tuberkulose gesichert, sondern zugleich bestimmte Resistenzgene nachgewiesen werden. In der Breite verfügbar sind zumindest Tests auf eine Rifampicin- und Isoniazid-Resistenz. In spezialisierten Laboren sind auch andere Antibiotikaresistenzen überprüfbar. Sollte ein Resistenzrisiko bestehen, empfiehlt sich bereits zu Beginn der Therapie eine molekularbiologische Testung zumindest auf eine Rifampicinresistenz, um eine MDR-Tuberkulose ausschließen zu können.
Aufgrund der Hepatoxizität der meisten Standardtherapeutika, der ggf. notwendigen Dosisadaptation bei Niereninsuffizienz und möglichen Blutbildveränderungen unter Therapie sind entsprechende Laborkontrollen in regelmäßigen Abständen obligat. Die Leitlinie gibt hierfür praktische Anleitungen [7]. Der Einsatz von EMB macht regelmäßige ophthalmologische Kontrollen erforderlich. Unter Aminoglykosiden muss auf nephro- und ototoxische Nebenwirkungen geachtet werden.
Risikofaktoren
Die Herkunft aus einem Hochinzidenzland (bspw. Subsahararaum, südostasiatischer Raum) ist der wichtigste Risikofaktor für die Entwicklung einer aktiven Tuberkulose. Danach kommen Abhängigkeitserkrankungen und Immunsuppression durch HIV oder Medikamente (Therapie mit TNFɑ-Blockern und anderen Biologicals, schwere Niereninsuffizienz, HIV-Infektion, Mangelernährung, Diabetes mellitus, Rauchen und Alkohol). Die Beschäftigung in Einrichtungen des Gesundheitswesens mit erhöhter Tuberkuloseprävalenz (wie Gefängnisse, Lungenkliniken oder -abteilungen etc.) ist mit einem marginalen zusätzlichen Risiko verbunden. Kinder unter vier Jahren sind besonders empfänglich für die Erkrankung, weshalb für Kinder Besonderheiten bei der Chemoprophylaxe zu beachten sind [7].
Übertragung und Infektionsprävention
Die Übertragung der Tuberkulose erfolgt fast ausschließlich aerogen von Mensch zu Mensch durch Erkrankte mit einer Lungentuberkulose, wobei das Ansteckungsrisiko mit der Dauer des Kontaktes und der Menge der ausgehusteten Bakterien korreliert [9]. Die Erregerzahl hängt vom Ausmaß des Lungenbefalls (z. B. Kaverne), der klinischen Symptomatik (vor allem dem Husten) und vor allem von der Stärke des Hustenstoßes ab. Die größte Ansteckungsgefahr geht daher von einem stark hustenden Patienten mit einer mikroskopisch offenen Lungentuberkulose aus. Wesentlich geringer ist diese Gefahr, wenn lediglich kulturell Mykobakterien im Sputum oder Bronchialsekret angezüchtet werden können oder die Erkrankten nicht husten. Bei der mikroskopisch offenen Tuberkulose gilt ein enger Raumkontakt von acht Stunden, bei ausschließlich kulturellem Erregernachweis von 40 Stunden als besonders gefährdend. Diese Zeiträume sind auch Grundlage für die Umgebungsuntersuchungen durch den öffentlichen Gesundheitsdienst. In besonderen Situationen (z. B. Reanimation, Bronchoskopie etc.) kann ein kürzerer Kontakt für eine Infektion ausreichen.
Äußerst seltene Infektionswege sind die Ingestion von erregerhaltigem Material (z. B. Milch bei der Rindertuberkulose), eine kongenitale Übertragung sowie theoretisch auch die Inokulation von bakterienhaltigem Wundsekret. Epidemiologisch spielt dies allerdings keine Rolle.
Ziel der Infektionsprävention ist daher die Vermeidung einer aerogenen Übertragung des Erregers. Es muss abgeklärt werden, ob ein pulmonaler Befall vorliegt und ob Infektiosität besteht. Eine Röntgenuntersuchung der Thoraxorgane und eine Untersuchung auf säurefeste Stäbchen im Sputum sind hierfür obligat.
Infektiöse Patienten sind zu isolieren. Grundsätzlich ist solange Infektiosität zu unterstellen, bis eine Sputumkonversion (dreimalig negative Sputummikroskopie an unterschiedlichen Tagen) eingetreten ist. In der Regel nimmt die Infektiosität unter einer dreiwöchigen Standardtherapie in dem Maße ab, dass bei der unkomplizierten Erkrankung keine Ansteckungsgefahr mehr anzunehmen ist.
Neben der räumlichen Isolierung des Patienten ist der Schutz des Personals und von Besuchern zu beachten. Für Deutschland werden Atemschutzmasken der Klasse FFP2 für Personal- und Besucher bei Betreten des Patientenzimmers empfohlen. Der einfache chirurgische Mund-Nasenschutz wird nicht mehr empfohlen, er soll lediglich vom Patienten beim Verlassen des Zimmers getragen werden (Verhinderung der Aerosolausbreitung). Der Patient selbst muss über alle diese Hygienemaßnahmen aufgeklärt werden.
Patienten mit rein extrapulmonaler Tuberkulose sind in der Regel nicht ansteckend. Auch wenn Erreger über den Urin oder andere Körperflüssigkeiten ausgeschieden werden, stellt dies bei entsprechenden Verhaltensweisen keine Gefahr dar. Ausführliche Informationen zur Infektionsprävention finden sich in den aktuellen Empfehlungen des Deutschen Zentralkomitees zur Bekämpfung der Tuberkulose [9].
Meldepflicht
Originalwortlaut des Infektionsschutzgesetzes: Meldepflichtig sind nach § 6 (1) 1. Infektionsschutzgesetz (IfSG) Erkrankung und Tod an einer behandlungsbedürftigen Tuberkulose, auch wenn ein bakteriologischer Nachweis nicht vorliegt.
Darüber hinaus ist nach § 6 (2) dem Gesundheitsamt zu melden, wenn Personen, die an einer behandlungsbedürftigen Lungentuberkulose leiden, eine Behandlung verweigern oder abbrechen.
Aufgaben der Gesundheitsämter sind die Ermittlung der Kontaktpersonen, Empfehlungen zur Prophylaxe und präventiven Therapie sowie die Therapieüberwachung. Zeichnen sich Probleme hinsichtlich der Therapietreue ab, besteht die Möglichkeit zur überwachten Medikamenteneinnahme (directly observed treatment DOT). Es ist eine enge Zusammenarbeit zwischen behandelndem Arzt und öffentlichem Gesundheitsdienst entscheidend für den Therapieerfolg.
Fazit
Die Tuberkulose ist in Deutschland mittlerweile eine relativ seltene Erkrankung geworden. Sie wird allerdings auch in Zukunft nicht völlig verschwinden und insbesondere bei Risikogruppen anzutreffen sein. Die Tuberkulose muss daher immer als mögliche Differenzialdiagnose bedacht werden. Im Zweifel sollten erfahrene pneumologische oder infektiologische Zentren bzw. Fachabteilungen hinzugezogen werden.
Dr. med. Christian Reinhardt, Prof. Dr. med. Stefan Andreas, Dr. med. Peter Hammerl, Lungenfachklinik Immenhausen, Pneumologische Lehrklinik Universität Göttingen, Zentrum für Pneumologie Nordhessen
Kontakt zu den Autoren per E-Mail: christian.reinhardt@lungenfachklinik-immenhausen.de
Die CME-Fragen und Literaturhinweise finden Sie in der PDF-Version der aktuellen Ausgabe auf unserer Website unter www.laekh.de/heftarchiv/ausgabe/2020/maerz-2020
Multiple Choice-Fragen
Die Multiple Choice-Fragen zu dem Artikel „Tuberkulose – in Deutschland wieder relevant!“ von Dr. med. Christian Reinhardt, Prof. Dr. med. Stefan Andreas und Dr. med. Peter Hammerl finden Sie im Mitglieder-Portal der Landesärztekammer Hessen (https://portal.laekh.de) sowie auf den Online-Seiten des Hessischen Ärzteblattes. Die Teilnahme zur Erlangung von Fortbildungspunkten ist ausschließlich online über das Mitglieder-Portal vom 25. Februar 2020 bis 24. Februar 2021 möglich.
Die Fortbildung ist mit zwei Punkten zertifiziert. Mit Absenden des Fragebogens bestätigen Sie, dass Sie dieses CME-Modul nicht bereits an anderer Stelle absolviert haben.
Dieser Artikel hat ein Peer-Review-Verfahren durchlaufen. Laut der Autoren sind die Inhalte des Artikels produkt- und/oder dienstleistungsneutral, es bestehen keine Interessenkonflikte.